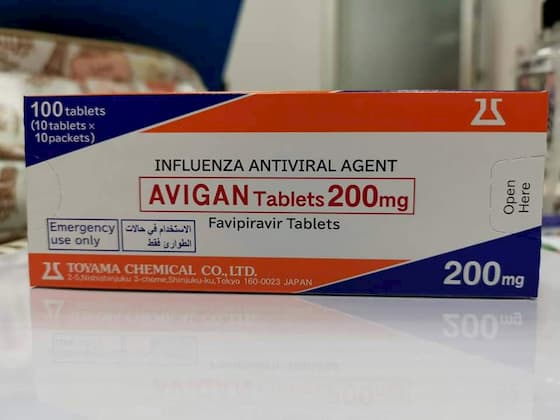
AVIGAN là một loại thuốc chỉ được xem xét sử dụng khi có sự bùng phát của các ca nhiễm vi rút cúm mới (thuốc điều trị covid-19) hoặc tái phát trong đó các tác nhân chống vi rút cúm khác không có hiệu quả hoặc quyết định sử dụng thuốc như một biện pháp đối phó với những loại vi rút cúm như vậy.
Khi sử dụng thuốc, hãy lấy thông tin mới nhất bao gồm chỉ đạo của chính phủ về các biện pháp đối phó với các loại vi rút cúm như vậy và chỉ kê đơn cho những bệnh nhân thích hợp, điều trị covid-19, diệt vi rút corona, sar-covi-2.
AVIGAN không được sử dụng cho các trường hợp nhiễm vi rút cúm mới hoặc đang tái phát. Thông tin về phản ứng có hại và kết quả nghiên cứu lâm sàng trong tờ hướng dẫn sử dụng thuốc này dựa trên các nghiên cứu lâm sàng của Nhật Bản với mức liều thấp hơn liều lượng đã được phê duyệt và các nghiên cứu lâm sàng ở nước ngoài. Nhật Bản đã cấp phép Avigan đều trị cho bệnh nhân nhiễm vi-rút corona, Sar-covi-2, bệnh covid-19
Thành phần / hàm lượng mỗi viên: Favipiravir 200mg
Thành phần tá dược: Povidone, silicon dioxide dạng keo, hydroxypropyl cellulose được thay thế thấp, crospovidone, natri stearyl fumarate, hypromellose, titanium dioxide, talc, oxit sắt màu vàng.
DƯỢC LỰC HỌC
Khi favipiravir được dùng bằng đường uống cho 20 đối tượng nam giới trưởng thành khỏe mạnh với liều 1200 mg x 2 lần / ngày trong 1 ngày, tiếp theo là 800 mg x 2 lần / ngày trong 4 ngày (1200 mg / 800 mg BID). Chú ý 7, nồng độ trung bình hình học của thuốc trong tinh dịch là 18.341 ig / mL vào ngày thứ 3 và 0,053 ig / mL vào ngày thứ hai sau khi điều trị. Nồng độ tinh dịch trở xuống dưới giới hạn định lượng (0,02 ig / mL) ở tất cả các đối tượng trong 7 ngày sau khi kết thúc điều trị. Tỷ lệ trung bình của nồng độ thuốc trong tinh dịch so với trong huyết tương là 0,53 vào ngày thứ 3 và 0,45 vào ngày thứ hai sau khi điều trị, đặc biệt điều trị covid-19
Lưu ý Liều lượng được chấp thuận của favipiravir là “1600mg uống hai lần mỗi ngày trong 1 ngày, sau đó là 600 mg uống hai lần mỗi ngày trong 4 ngày”.
Tỷ lệ liên kết protein huyết thanh là 53,4 đến 54,4% (trong ống nghiệm, siêu lọc ly tâm) ở 0,3 đến 30 ig / mL
CHỈ ĐỊNH THUỐC AVIGAN 200mg
Nhiễm vi-rút cúm mới hoặc tái phát (chỉ giới hạn trong các trường hợp mà các tác nhân chống vi-rút cúm khác không hiệu quả hoặc không hiệu quả)
Điều trị cho bệnh nhân nhiễm vi-rút corona, covid-19
Các biện pháp phòng ngừa
AVIGAN là loại thuốc chỉ được xem xét sử dụng khi có đợt bùng phát nhiễm vi rút cúm mới hoặc tái phát trong đó các tác nhân chống vi rút cúm khác không hiệu quả hoặc không hiệu quả và chính phủ quyết định sử dụng thuốc như một biện pháp đối phó với những vi rút cúm như vậy. Thuốc điều trị covid-19, diệt corona virus, sar-covi-2. Khi sử dụng thuốc, hãy lấy thông tin mới nhất bao gồm chỉ đạo của chính phủ về các biện pháp đối phó với các loại vi rút cúm như vậy và chỉ kê đơn cho những bệnh nhân thích hợp.
AVIGAN không có hiệu quả đối với các bệnh nhiễm trùng do vi khuẩn.
AVIGAN chưa được sử dụng cho trẻ em.
CHỐNG CHỈ ĐỊNH THUỐC AVIGAN 200mg
– Phụ nữ đã biết hoặc nghi ngờ có thai
Chết phôi sớm và gây quái thai đã được quan sát thấy trong các nghiên cứu trên động vật. Sử dụng trong thời kỳ mang thai, sinh nở hoặc cho con bú
– Bệnh nhân có tiền sử mẫn cảm với bất kỳ thành phần nào của thuốc
LIỀU LƯỢNG VÀ CÁCH DÙNG THUỐC AVIGAN 200mg
Liều thông thường của favipiravir cho người lớn là 1600 mg uống hai lần mỗi ngày trong 1 ngày, sau đó là 600 mg uống hai lần mỗi ngày trong 4 ngày. Tổng thời gian quản lý phải là 5 ngày.
Điều trị cho bệnh nhân nhiễm vi-rút corona ở người mắc COVID-19
CÁC BIỆN PHÁP PHÒNG NGỪA
Sử dụng cẩn thận
Bệnh nhân bị bệnh gút hoặc tiền sử bệnh gút và bệnh nhân bị tăng axit uric máu (Mức axit uric máu có thể tăng và các triệu chứng có thể trầm trọng hơn.
- Các biện pháp phòng ngừa quan trọng
(1) Chưa có nghiên cứu lâm sàng nào được thực hiện để kiểm tra tính hiệu quả và an toàn của AVIGAN với liều lượng đã được phê duyệt. Liều lượng được phê duyệt được ước tính dựa trên kết quả của một nghiên cứu lâm sàng giai đoạn I / II có đối chứng với giả dược ở bệnh nhân nhiễm vi rút cúm và dữ liệu dược động học từ các nghiên cứu ở Nhật Bản và ở nước ngoài. Sự gia tăng nồng độ favipiravir trong huyết tương đã được báo cáo ở những bệnh nhân suy giảm chức năng gan trong nghiên cứu dược động học được thực hiện bên ngoài Nhật Bản.
(2) Mặc dù mối quan hệ nhân quả chưa được biết, nhưng các triệu chứng tâm thần như hành vi bất thường sau khi sử dụng các tác nhân chống vi rút cúm bao gồm cả AVIGAN đã được báo cáo. Đối với việc điều trị cho trẻ em và trẻ vị thành niên, như một phương pháp phòng ngừa trong trường hợp tai nạn do hành vi bất thường như té ngã, bệnh nhân / gia đình họ nên được hướng dẫn rằng, sau khi bắt đầu điều trị bằng các chất chống vi rút cúm, (i) bất thường hành vi có thể được phát triển, và (ii) người giám hộ và những người khác nên sắp xếp để trẻ em / trẻ vị thành niên không bị bỏ lại một mình trong ít nhất 2 ngày khi chúng được điều trị tại nhà. Vì các triệu chứng tương tự liên quan đến bệnh não do cúm đã được báo cáo, nên hướng dẫn tương tự như trên.
(3) Nhiễm vi rút cúm có thể phức tạp với nhiễm vi khuẩn hoặc có thể bị nhầm lẫn với các triệu chứng giống cúm. Trong trường hợp nhiễm vi khuẩn hoặc nghi ngờ là nhiễm vi khuẩn, cần thực hiện các biện pháp thích hợp, chẳng hạn như sử dụng các chất chống vi khuẩn. Cần bổ xung thêm kinh nghiệm với thuốc điều trị covid-19
Tương tác thuốc
AVIGAN không được chuyển hóa bởi cytochrome P-450 (CYP), phần lớn được chuyển hóa bởi aldehyde oxidase (AO), và một phần được chuyển hóa bởi xanthine oxidase (XO). Thuốc ức chế AO và CYP2C8, nhưng không gây ra CYP.
Phản ứng có hại
AVIGAN chưa bao giờ được sử dụng với liều lượng đã được phê duyệt. Trong các nghiên cứu lâm sàng của Nhật Bản và nghiên cứu giai đoạn III toàn cầu (các nghiên cứu được thực hiện với liều lượng thấp hơn liều lượng đã được phê duyệt), phản ứng có hại đã được quan sát thấy ở 100 trong số 501 đối tượng (19,96%) được đánh giá về độ an toàn (bao gồm các giá trị thử nghiệm bất thường trong phòng thí nghiệm). Các phản ứng phụ chính bao gồm tăng axit uric máu
- Sốc, phản vệ
- Viêm phổi
- Viêm gan tối cấp, rối loạn chức năng gan, vàng da
- Hoại tử biểu bì nhiễm độc (TEN), hội chứng da mắt (hội chứng Stevens-Johnson)
- Tổn thương thận cấp tính
- Số lượng bạch cầu giảm, số lượng bạch cầu trung tính giảm, số lượng tiểu cầu giảm
- Các triệu chứng thần kinh và tâm thần (rối loạn ý thức, hành vi bất thường, mê sảng, ảo giác, ảo tưởng, co giật, v.v.)
- Viêm đại tràng xuất huyết.
Nếu các phản ứng phụ sau đây xảy ra, cần thực hiện các biện pháp thích hợp tùy theo các triệu chứng
- Sử dụng ở Người cao tuổi
Vì người cao tuổi thường bị suy giảm chức năng sinh lý, nên dùng AVIGAN một cách cẩn thận cho họ bằng cách theo dõi tình trạng chung của họ.
- Sử dụng trong thời kỳ mang thai, sinh nở hoặc cho con bú
(1) Không dùng AVIGAN cho phụ nữ đã biết hoặc nghi ngờ có thai.
(Chết phôi sớm [chuột] và gây quái thai [khỉ, chuột nhắt, chuột cống và thỏ] đã được quan sát thấy trong các nghiên cứu trên động vật với mức độ phơi nhiễm tương tự hoặc thấp hơn mức phơi nhiễm lâm sàng.)
(2) Khi dùng AVIGAN cho phụ nữ đang cho con bú, hãy hướng dẫn ngừng cho con bú.
(Chất chuyển hóa chính của AVIGAN, một dạng hydroxy lated, được tìm thấy là phân phối trong sữa mẹ.)
- Sử dụng cho trẻ em
AVIGAN chưa được dùng cho trẻ em.
- Các biện pháp phòng ngừa liên quan đến việc sử dụng
Đối với các loại thuốc được phân phối trong một gói ép qua (PTP), bệnh nhân nên được hướng dẫn để lấy thuốc ra khỏi gói trước khi sử dụng. (Có thông tin cho rằng, nếu nuốt phải tấm PTP, các góc nhọn của tấm có thể làm thủng niêm mạc thực quản, dẫn đến các biến chứng nặng như viêm trung thất.
Các biện pháp phòng ngừa khác
Trong các nghiên cứu trên động vật, những thay đổi mô bệnh học của tinh hoàn ở chuột cống (12 tuần tuổi) và chó non (7 đến 8 tháng tuổi), và những phát hiện bất thường về tinh trùng ở chuột nhắt (11 tuần tuổi) đã được báo cáo. Sự phục hồi hoặc xu hướng phục hồi đã được quan sát thấy trong những nghiên cứu đó sau khi ngừng sử dụng.
Bảo quản: cất giữ ở nhiệt độ phòng
Hãng sản xuất: TOYAMA CHEMICAL CO., LTD
Công ty phân phối: Taisho Toyama Pharmaceutical Co., Ltd.
3-25-1, Takada, Toshima-ku, Tokyo 170-8635, Japan Toll-Free: 0120-591-818
Chưa có bình luận.