U tủy thượng thận có thể gặp ở bất kỳ lứa tuổi nào nhưng thường gặp nhất ở độ tuổi 30 đến 50. Ở trẻ em, tỷ lệ mắc khoảng 10%. Mổ là giải pháp điều trị triệt để u tụy thượng thận.
U tủy thượng thận chiếm khoảng 0,1 % tổng số các trường hợp tăng huyết áp ở người lớn. U tủy thượng thận là các khối u tiết catecholmin bắt nguồn từ các tế bào ưa chrom trong tủy thượng thận. Mặc dù nó là nguyên nhân gây tăng huyết áp không phổ biến nhưng việc chẩn đoán có hay không có u tủy thượng thận ở bệnh nhân tăng huyết áp là điều bắt buộc vì nguy cơ tử vong cao và đó là một trong những thể tăng huyết áp có thể điều trị được thực sự.
Tăng tiết catecholamin không kiểm soát có thể gây tăng huyết áp ác tính, tai biến mạch máu não và nhồi máu cơ tim. Đó là những thách thức lớn cho bác sĩ gây mê cả trong phòng mổ cũng như tại đơn vị chăm sóc tích cực sau mổ. Trước những năm 1960, chưa có xét nghiệm sàng lọc nước tiểu và sử dụng các thuốc ức chế anpha adrenergic điều trị trước mổ, có khoảng 25 % đến 50% bệnh nhân (nội trú có u tủy thượng thận) tử vong khi khởi mê hoặc các rối loạn không liên quan trong khi mổ.
Nguyên nhân chính xác của u tủy thượng thận vẫn còn chưa rõ ràng. Khoảng 90% các trường hợp u tủy thượng thận được phát hiện mang tính chất tự phát, 10% mang tính chất di truyền gia đình khi có tính trạng trội của nhiễm sắc thể thường. Hai giới có tỷ lệ mắc như nhau, u tủy thượng thận có thể gặp ở bất kỳ lứa tuổi nào nhưng thường gặp nhất ở độ tuổi 30 đến 50. Ở trẻ em, tỷ lệ mắc khoảng 10%, các triệu chứng lâm sàng thường không đặc hiệu nên rất khó chẩn đoán. Các u tuyến thượng thận mang tính chất gia đình thường gặp là u tuyến ở cả hai bên hoặc các khối u ở ngoài tuyến thượng thận nhưng cùng vị trí giải phẫu xuất hiện ở các thế hệ kế tiếp trong gia đình.
Những tiến bộ gần đây cho phép chẩn đoán sớm u tủy thượng thận mang tính chất gia đình trước khi xuất hiện các triệu chứng lâm sàng nhờ chẩn đoán gen. U tủy thượng thận gia đình có thể là một phần của hội chứng u nhiều tuyến nội tiết và có liên quan tới loạn sản tế bào ngoại bì thần kinh. Các bệnh nhân có hội chứng u nhiều tuyến nội tiết nhóm 2a có u tủy thượng thận, ung thư nhân tuyến giáp và cường tuyến cận giáp. Các bệnh nhân nhóm 2b có u tủy thượng thận, ung thư nhân tuyến giáp, các u hạch thần kinh đường tiêu hóa, dày thần kinh giác mạc, hội chứng marfan.
Thường gặp u tủy thượng thận cả hai bên cơ thể và rất hiếm khi ác tính ở các bệnh nhân có hội chứng u nhiều tuyến nội tiết 2a và 2b. Gần như 100% bệnh nhân ở cả hai nhóm 2a và 2b có hoặc sẽ phát triển thành u tủy thượng thận lành tính 2 bên, loạn sản bì thần kinh. Khoảng 10% đến 25% bệnh nhân mắc hội chứng Von Hippel-Lindau (u mạch ở tiểu não và võng mạc) có thể có u tủy thượng thận; khoảng 1% bệnh nhân mắc bệnh Recklinghausen (u xơ thần kinh) có u tủy thượng thận, các bệnh nhân có xơ cứng rễ và hội chứng Sturge-Weber có u tủy thượng thận.
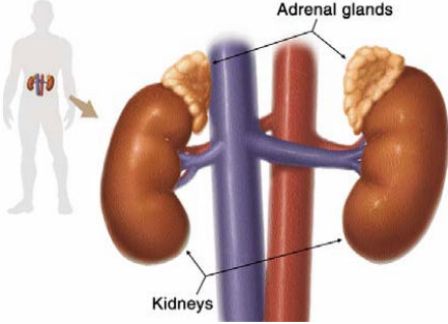
U ác tính tuyến thượng thận có thể di căn qua đường tĩnh mạch tới các cơ quan chiếm ưu thế như gan và xương, mặc dù tủy sống, phổi não và các hạch bạch huyết cũng có thể bị. Nhìn đại thể bề ngoài các khối di căn như một khối u lành tính. Tỷ lệ ác tính khoảng 10%, tỷ lệ này có thể tăng cao do ngày càng tiến bộ trong các phương tiện chẩn đoán trong tương lai. Tỷ lệ sống trên 5 năm với u ác tính tủy thượng thận là 44%, khoảng 5% – 10% có tái phát sau khi cắt u tủy thượng thận lành tính.
Khoảng 80% các khối u tủy thượng thận khu trú ở tủy thượng thận, bên phải thường bị nhiều hơn bên trái. Khoảng 20% u tuyến thượng thận khu trú ở ngoài tuyến thượng thận (lạc chỗ), chủ yếu là trong ổ bụng và liên quan tới hạch giao cảm. Các vị trí giải phẫu gần chỗ chia nhánh của động mạch chủ là vị trí thường gặp nhất của u tuyến thượng thận lạc chỗ, khoảng 2% lạc chỗ lên ngực và cổ. Khoảng 10% các u tủy thượng thận gặp ở trẻ em, trong đó có 30 % bệnh nhân có nhiều khối u, 30% có khối u lạc chỗ, 20% có u thượng thận hai bên và gặp ở trẻ em nhiều hơn người lớn.
Sự phát triển của u tuyến thượng thận lạc chỗ được giải thích do không có khả năng teo nhỏ các mô ưa chrome ở thời thơ ấu. Trái ngược với sự hiểu biết trước đây, hầu hết các u tủy thượng thận lạc chỗ có quá trình tiến triển lành tính. Các u tuyến thượng thận ở người trưởng thành có đặc điểm là khối đặc, giàu mạch máu, đường kính từ 3-5 cm, trọng lượng trung bình 100 g (dao động từ 1 – 4000 g). Các khối u có kích thước lớn ở người trưởng thành có thể chứa từ 100-800 mg norepinephrin.
Các u tủy thượng thận là các u của hệ thần kinh giao cảm. Hệ thần kinh giao cảm còn nguyên vẹn và hoạt động cùng sự hiện diện của khối u. Các biểu hiện lâm sàng của u tủy thượng thận là kết quả giải phóng hormon của khối u. Hầu hết các khối u tủy thượng thận tiết ra mình norepinephrin, hoặc phổ biến hơn là tiết cùng một lượng nhỏ epinephrin với tỉ lệ 85:15, tuyến thượng thận bình thường tiết ra hormon với tỉ lệ đảo ngược (15:85). Có khoảng 15% khối u tiết epinephrin nhiều hơn, một số tiết ra cả dopamin. Hầu hết các u tủy thượng thận tiết catecholamin một cách tự động mà không bị kiểm soát bởi hệ thần kinh.
Triệu chứng lâm sàng
Tăng huyết áp liên tục hoặc kịch phát là biểu hiện thường xuyên nhất của u tuyến thượng thận. Các triệu chứng kinh điển gồm:
+ Đau đầu
+ Vã mồ hôi,
+ Xanh sao và đánh trống ngực.
Hầu hết bệnh nhân có các triệu chứng và sự bùng phát, phạm vi thay đổi từ không thường xuyên (một lần một tháng hoặc ít hơn) cho đến dữ dội (nhiều lần một ngày), có thể kéo dài từ vài phút đến vài giờ. Các triệu chứng có thể tự phát hoặc được thúc đẩy khi tăng hoạt động thể lực hoặc kích thích tâm lý hoặc các thuốc. Tăng huyết áp gặp ở trên 80% bệnh nhân trưởng thành. Tăng huyết áp kịch phát xen giữa các giá trị huyết áp bình thường xảy ra ở khoảng 50% bệnh nhân, khoảng 30% bệnh nhân có biểu hiện tăng huyết áp liên tục. Theo dõi huyết áp liên tục 24 giờ trên monitor cho thấy nhiều cơn tăng huyết áp mà không có triệu chứng. Hạ huyết áp tư thế cũng là một dấu hiệu thường gặp và được coi là giảm thể tích tuần hoàn thứ phát do giảm đáp ứng với phản xạ co động, tĩnh mạch với các chất co mạch. Các dấu hiệu về huyết động tùy thuộc vào loại catecholamin nào tiết ra chiếm ưu thế. Khi norepinephrin được tiết ra nhiều hơn, tác dụng anpha-adrenergic mạnh hơn nên bệnh nhân có biểu hiện tăng huyết áp tâm thu và tâm trương cùng với phản xạ chậm nhịp tim. Khi u tuyến thượng thận tiết nhiều epinephrin hơn, tác dụng beta-adrenergic là chủ yếu nên có biểu hiện tăng huyết áp tâm thu, hạ huyết áp tâm trương và nhịp tim nhanh.
Một số bệnh nhân có huyết áp bình thường mặc dù có mức norepinephrin cao trong hệ tuần hoàn. Ở bệnh nhân u tủy thượng thận việc điều chỉnh huyết áp động mạch phức tạp hơn các quan điểm truyền thống. Mức tăng huyết áp động mạch dường như có ít liên quan với mức catecholamin đang lưu hành trong hệ tuần hoàn. Nguyên nhân có thể do sự mất cân bằng giữa các chất giãn mạch nội sinh (như dopamin, serotonin, enkephalin và các chất vận mạch ở ruột) và các catecholamin trong hệ tuần hoàn. Mặc dù mức catecholamin trong hệ tuần hoàn có thể cao hơn gấp hàng chục lần ở các bệnh nhân u tủy thượng thận nhưng sự biến đổi huyết động không có khác biệt đáng kể so với các bệnh nhân cao huyết áp nguyên phát. Cả hai loại này đều có tăng sức kháng thành mạch, cung lượng tim vẫn bình thường, nhưng có giảm nhẹ thể tích huyết tương.
Sự tăng cao của catecholamin trong huyết tương lâu dài không gây ra đặc điểm đặc trưng trong đáp ứng huyết động cấp tính. Điều này có thể do giảm sự nhạy cảm của hệ tim mạch hoặc giảm sự điều hòa các receptor adrenergic. Giảm sự nhạy cảm thứ phát của các tế bào cơ trơn do giảm số lượng các receptor hoặc thay đổi ở khớp nối thần kinh cơ. Tuy nhiên, sự đáp ứng huyết động của các cơn tăng huyết áp xảy ra tương tự như tăng cấp tính catecholamin. Mạch máu của các bệnh nhân u tủy thượng thận thường cần một nồng độ catecholamin rất cao mới có đáp ứng co mạch tăng huyết áp.
Bệnh cơ tim có thể làm giảm đáp ứng của tim với catecholamin. Tác động thực sự của bệnh cơ tim tới các triệu chứng lâm sàng còn chưa rõ ràng. Giảm toàn bộ chức năng bơm của cơ tim do giảm mạng lưới các nguyên bào trong cơ tim và giảm sự điều hòa của các receptor beta. Nguyên nhân do nhiều yếu tố gây ra bao gồm thay đổi giảm tính thấm của catecholamin qua màng tế bào dẫn tới tăng ồ ạt ion calci, nhiễm độc các sản phẩm oxi hóa catecholamin, gây nguy hại cho các gốc tự do. Hơn nữa, nồng độ catecholamin cao ảnh hưởng lên tim thông qua sự co động mạch vành vì tác động lên receptor anpha-adrenergic, gây giảm dòng máu vành và nguy cơ thiếu máu cơ tim.
Cả bệnh cơ tim thể giãn và phì đại cơ tim cũng như tắc nghẽn dòng máu về tim trái đã được đánh giá qua siêu âm tim. Kết quả cho thấy siêu âm tim bình thường ở những bệnh nhân không có các triệu chứng ở hệ tim mạch (khó thở, đau ngực) hoặc các dấu hiệu lâm sàng khác có liên quan đến tim. Điện tim bất thường có thể gồm sự chênh lênh hoặc lõm xuống của đoạn ST, sóng T đảo ngược hoặc nằm ngang, kéo dài khoảng QT, sóng P cao, trục chuyển trái và rối loạn nhịp. Những sự thay đổi này mang tính thoáng qua, có thể thay đổi và trở lại bình thường với các thuốc ức chế anpha và hoặc thuốc ức chế beta.
Bệnh cơ tim có thể được hồi phục nếu loại bỏ được các kích thích catecholamin trước khi xảy ra xơ hóa các nguyên bào sợi cơ tim. Khác với bệnh cơ tim, các bệnh u tủy thượng thận có thể dẫn tới suy tim xung huyết có phì đại cơ tim thứ phát do tăng huyết áp liên tục. Vì các u tủy thượng thận có sự thay đổi rõ ràng trong hoạt động bài tiết hormon, có thể nhầm lẫn với nhiễm độc giáp, tăng huyết áp ác tính, đái đường, hội chứng ung thư hạch hoặc nhiễm khuẩn gram âm. Các bệnh nhân u tủy thượng thận hiếm khi có mức đường máu bình thường, hầu hết đều tăng đường máu thứ phát do catecholamin kích thích tổng hợp phân giải glycogen và ức chế bài tiết insulin.
Chẩn đoán bệnh u tủy thượng thận
Khi lâm sàng có nghi ngờ u tủy thượng thận cần làm định lượng catecholamin. Có nhiều các xét nghiệm được sử dụng để chẩn đoán u tủy thượng thận nhưng không có xét nghiệm nào là lý tưởng. Dù có lựa chọn làm xét nghiệm nào chăng nữa cũng cần kiểm soát chặt chẽ các tình huống trong lâm sàng (như tập thể dục, sự xúc động, sử dụng các thuốc) để có kết quả đáng tin cậy. Một số yếu tố như uống rượu, nhược giáp, giảm thể tích máu… có thể làm sai lệch các kết quả xét nghiệm chẩn đoán u tủy thượng thận.
Xét nghiệm nhạy cảm nhất cho các bệnh nhân có nguy cơ cao (u tủy thượng thận gia đình hoặc có các triệu chứng điển hình) là định lượng các chất chuyển hóa tự do của catecholamin trong huyết tương. Các catecholamin bị chuyển hóa thành các chất chuyển hóa tự do trong các tế bào của khối u, các chất chuyển hóa này được phóng thích liên tục vào hệ tuần hoàn. Chẩn đoán u tủy thượng thận khi xét nghiệm normetanephrine lớn hơn 400 pg/mL và hoặc metanephrine lớn hơn 220 pg/mL trong huyết tương. Nghi ngờ chẩn đoán nếu giá trị của normetanephrine từ 112 -400 pg/mL hoặc metanephrine từ 61 – 220 pg/mL. Loại trừ u tủy thượng thận nếu normetanephrine thấp hơn 112 pg/mL và metanephrine thấp hiwn 61 pg/mL.
Xét nghiệm catecholamin tự do trong nước tiểu và các chất chuyển hóa của nó (như metanephrine, normetanephrine, acid vanillylmandelic) cũng thường được sử dụng để chẩn đoán u tủy thượng thận. Xét nghiệm rất dễ thực hiện và có sẵn, tuy nhiên việc thu thập nước tiểu 24 giờ không tiện lợi và không đáng tin cậy. Định lượng acid vanillylmandelic (chất chuyển hóa cuối cùng của catecholamin) là xét nghiệm rẻ và kinh điển nhất nhưng không đặc hiệu. Xác định mức tăng cao của metanephrin là xét nghiệm nước tiểu tốt nhất. Với những bệnh nhân ít có khả năng bị u tủy thượng thận, chỉ cần xét nghiệm định lượng metanephrine và catecholamines nước tiểu 24 giờ là đủ.
Định lượng chính xác nồng độ catecholamin huyết tương là xét nghiệm đầu tiên được chỉ định. Một số lượng lớn bệnh nhân có tăng đáng kể norepinephrin, epinephrin hoặc cả hai, mặc dù một vài bệnh nhân u tủy thượng thận có nồng độ catecholamin bình thường lúc nghỉ. Chẩn đoán xác định u tủy thượng thận khi tổng nồng độ catecholamin huyết tương lớn hơn 2000 pg/mL. Nghi ngờ khi giá trị tổng lượng catecholamin nằm trong khoảng từ 500 đến 2000 pg/mL và loại trừ khi giá trị thấp hơn 500 pg/mL. Trong phần lớn các trường hợp, sự tăng cao catecholamin ở cả huyết tương hoặc catecholamin tự do và các chất chuyển hóa của nó trong nước tiểu đủ thỏa mãn để chẩn đoán xác định. Kết quả không rõ ràng trong 5-10% số bệnh nhân và trong những trường hợp này, sử dụng test “ngăn chặn” bằng clonidin. Clonidin là thuốc ức chế anpha 2 tác động trên hệ thống thần kinh trung ương để giảm bớt hoạt động của giao cảm ly tâm.
Ở những bệnh nhân u tủy thượng thận, nồng độ catecholamin tăng trong huyết tương do khối u tăng tiết, bỏ qua cơ chế tiết và lưu giữ bình thường. Clonidin tác dụng làm giảm catecholamin huyết tương ở những bệnh nhân không có u tủy thượng thận trong khi không có tác dụng hạ catecholamin ở bệnh nhân u tủy thượng thận.
Trước đây, sử dụng test kích thích tăng tiết catecholamin từ khối u bằng histamin và tyramin. Tuy nhiên, điều này làm tăng tỷ lệ biến chứng và tử vong nên hiện nay đã bị cấm sử dụng. Test kích thích bằng glucagon hiện nay được coi là an toàn nhất và là test kích thích đặc hiệu nhất. Glucagon tác động trực tiếp lên khối u để giải phóng catecholamin. Xét nghiệm này ở những bệnh nhân có huyết áp tâm thu thấp hơn 100 mmHg. Test được coi là dương tính nếu catecholamin huyết tương tăng ít nhất ba lần so với giá trị ban đầu hoặc tăng cao hơn 2000 pg/mL trong vòng từ 1-3 phút tiêm glucagon. Hiện nay, hầu hết các trung tâm chẩn đoán u tủy thượng thận bằng xét nghiệm nước tiểu định lượng catecholamin tự do và chất chuyển hóa của nó hoặc xét nghiệm mức catecholamin huyết tương, sử dụng test clonidin hoặc test kích thích bằng glucagon ở những trường hợp nghi ngờ. Trong số các test này, xét nghiệm nào là đáng tin cậy nhất vẫn còn đang gây tranh cãi.
Vị trí khối u có thể được dự đoán dựa vào tính chất catecholamin tiết ra (bảng 1). Các xét nghiệm chẩn đoán hình ảnh chuyên biệt có thể cho biết vị trí chính xác khối u. Chụp cắt lớp vi tính (CT) và cộng hưởng từ (MRI) là các phương pháp chẩn đoán không xâm lấn tối ưu cho phép xác định vị trí giải phẫu của u tủy thượng thận. CT xác định được trên 95% các khối u tủy thượng thận có đường kính lớn hơn 1cm. MRI có nhiều ưu điểm hơn CT vì phân biệt được các tổn thương nhỏ hơn của tuyến thượng thận, phân biệt tốt hơn các tổn thương khác nhau của tuyến thượng thận, không cần dùng chất cản quang tĩnh mạch, không bị phơi nhiễm với tia xạ. Trên chuỗi hình ảnh MRI, u tủy thượng thận có cường độ tín hiệu cao và tăng sáng. CT và MRI cung cấp các thông tin chủ yếu về mặt giải phẫu, ngược lại xạ hình ký bằng meta-iodobenzylguanidin đánh dấu bằng iod 131 và iod 123 (131I-MIBG và 123I-MIBG) lại cung cấp nhiều thông tin về mặt chức năng. MIBG là đồng phân của guanethidin, có cấu trúc tương tự norepinephrin, bị bắt giữ ở các neuron adrenergic và tập trung ở các khối u tiết catecholamin. MIBG được xác định qua xạ hình. Đây là một xét nghiệm mang tính chất sinh lý học qua đó để xác định vị trí khối u thượng thận dựa trên hoạt động dược lý học. Nó rất có hiệu quả trong việc xác định các khối u tủy thượng thận lạc vị trí, các khối di căn và khẳng định khối thượng thận có chức năng của u tủy thượng thận. MIBG cho phép quan sát toàn bộ cơ thể và là lựa chọn hàng đầu để xác định vị trí khối u tủy thượng thận. CT, MRI và xạ hình ký 131I-MIBG là các thăm khám bổ sung để xác định vị trí khối u tủy thượng thận. Có thể đặt catheter chọn lọc để định lượng catecholamin máu tĩnh mạch thượng thận so sánh với catecholamin của máu tĩnh mạch các vị trí khác cũng là một xét nghiệm có ích.
Vô cảm cho phẫu thuật
– Giai đoạn chuẩn bị trước mổ u tủy thượng thận
Không có các nghiên cứu có kiểm soát, tiến cứu ngẫu nhiên về ý nghĩa của việc ức chế hệ adrenergic ở những bệnh nhân u tủy thượng thận ở giai đoạn trước trong và sau mổ. Tuy nhiên, việc đưa vào sử dụng các thuốc ức chế anpha-adrenergic trong giai đoạn trước mổ, tỷ lệ tử vong sau cắt tủy thượng thận đã giảm từ 40% – 60% năm 1951 xuống 0% – 6% năm 1967. Kết quả này mang lại nhiều thuận lợi cho quá trình vô cảm và theo dõi vô cảm. Một số tác giả thấy sử dụng các thuốc tác dụng nhanh có ích lợi hơn sử dụng các thuốc ức chế anpha. Vì hầu hết các khối u tủy thượng thận tiết ra nhiều norepinephrin hơn epinephrin, điều trị nội khoa thuốc ức chế anpha làm hạ huyết áp, tăng thể tích nội mạch, ngăn ngừa các cơn tăng huyết áp kịch phát, làm tăng sự nhạy cảm của các receptor adrenergic và giảm rối loạn chức năng cơ tim. Mặc dù có thể u tủy thượng thận có thể kèm theo giảm đáng kể thể tích nội mạch, đa số các bệnh nhân có thể tích nội mạch bình thường hoặc giảm nhẹ.
Các thuốc ức chế anpha có tác dụng bảo vệ hiệu quả co bóp cơ tim và việc tưới máu mô từ các tác dụng bất lợi của catecholamin. Phenoxybenzamin là thuốc ức chế anpha được sử dụng thường xuyên nhất giai đoạn trước mổ. Nó là thuốc ức chế không cạnh tranh chủ vận anpha 1 và có một số thuộc tính ức chế anpha 2. Vì là một chất ức chế không cạnh tranh nên nó rất khó để ức chế hết các catecholamin dư thừa. Phenoxybenzamin có thời gian tác dụng dài nên chỉ cần uống hai lần một ngày. Liều khởi đầu thường là 10 -20 mg, 2 lần mỗi ngày, hầu hết các bệnh nhân cần tới 60 – 250 mg /ngày. Mục tiêu điều trị là đưa huyết áp về bình thường, làm hết cá triệu chứng, hết sự biến đổi sóng ST và sóng T trên điện tim đồ và loại trừ rối loạn nhịp tim.
Điều trị quá liều có thể gây hạ huyết áp tư thế đứng. Khoảng thời gian điều trị ức chế anpha bao lâu là tối ưu vẫn còn là dấu hỏi, nhìn chung dao động từ 2 đến 3 tuần hoặc lâu hơn. Bởi vì nó có tác dụng kéo dài trên receptor anpha nên khuyến cáo ngừng thuốc 24 đến 48 giờ trước phẫu thuật để tránh việc mất đáp ứng của mạch máu ngay sau khi lấy bỏ khối u. Một số bác sĩ gây mê chỉ sử dụng một nửa hoặc 2/3 liều buổi sáng trước cuộc mổ để có tác dụng tương tự. Trong khi phẫu thuật viên yêu cầu ngừng thuốc 48 giờ trước phẫu thuật để họ sử dụng việc tăng huyết áp trong mổ như là tín hiệu để xác định các khối u di căn. Tuy nhiên, cho dù có dùng đầy đủ các thuốc ức chế anpha trước mổ thì tăng huyết áp vẫn xảy ra khi kích thích bằng tay vào khối u. Nhưng do ức chế thụ cảm thể anpha 1 và anpha 2, phenoxybenzamin làm tăng tiết catecholamin thông qua việc ức chế anpha 2 gây nhịp tim nhanh.
Prazocin là thuốc ức chế cạnh tranh chọn lọc anpha 1 có thể được sử dụng thay thế phenoxybenzamin. Nó có thời gian tác dụng ngắn hơn, ít gây tăng nhịp tim hơn và dễ chuẩn độ hơn phenoxybenzamin. Liều khởi đầu là 1 mg, dùng 3 lần mỗi ngày, có thể tăng liều tới 8-12 mg/ngày để đạt được tác dụng mong muốn. Một số ý kiến cho rằng nó không ngăn chặn đầy đủ các cơn tăng huyết áp ở giai đoạn trước phẫu thuật mặc dù có nhiều ý kiến ủng hộ việc sử dụng prazocin. Các thuốc ức chế anpha 1 khác bao gồm doxazosin và terazosin. Doxazosin sử dụng liều từ 2 -6 mg/ngày có hiệu quả kiểm soát tăng huyết áp như phenoxybenzamin và gây ít tác dụng không mong muốn hơn ở giai đoạn trước mổ (nhịp tim nhanh) và sau mổ (giảm huyết áp) cắt bỏ khối u.
Sử dụng các thuốc ức chế beta-adrenergic thay thế nếu nhịp tim nhanh (>120 nhịp/phút) hoặc xuất hiện các rối loạn nhịp tim do tác dụng ức chế anpha 2 từ phenoxybenzamin. Các thuốc ức chế chọn lọc beta-adrenergic không bao giờ được sử dụng trước các thuốc ức chế anpha vì ức chế tác dụng giãn mạch của receptor beta 2 gây ra mất đối kháng với chủ vận anpha dẫn tới co mạch và tăng huyết áp. Propranolol là thuốc ức chế không chọn lọc beta 1, beta 2 có thời gian bán thải trên 4 giờ thường được sử dụng nhất. Hầu hết các bệnh nhân cần tới 80-120 mg/ngày. Một số bệnh nhân có u tủy thượng thận tiết ra epinephrin liều có thể dùng tới 480 mg/ngày.
Các thuốc ức chế beta cần được sử dụng một cách cẩn trọng vì dù liều thấp nhưng có một số đáng kể bệnh nhân xuất hiện suy tim xung huyết hoặc bệnh lý cơ tim khi đã có sẵn các bệnh lý này nhưng ở trạng thái tiềm tàng. Atenolol, metoprolol và labetalol đã được sử dụng có hiệu quả, mặc dù kinh nghiệm về các thuốc này vẫn còn hạn chế và có một số thông báo biến chứng về sau. Labetalol gây ra mức độ ức chế anpha và beta (tác dụng ức chế beta nhiều hơn anpha) có thể không thích hợp cho bệnh nhân u tủy thượng thận. Rất ít khi lựa chọn sử dụng các thuốc ức chế beta trước khi sử dụng thuốc ức chế anpha. Với bệnh nhân u tủy thượng thận tiết ra epinephrin đơn thuần và có bệnh lý động mạch vành có thể có lợi ích lớn hơn khi dùng thuốc ức chế chọn lọc receptor beta 1 như esmolol. Esmelol có thời gian khởi phát tác dụng nhanh và thời gian bán thải ngắn, có thể dử dụng tiêm tĩnh mạch ngay trước khi phẫu thuật.
α-Methylparatyrosine (metyrosine) ức chế việc kiểm soát tốc độ quá trình tổng hợp catecholamin, làm giảm 50% đến 80% lượng catecholamin được tạo ra. Liều sử dụng thay đổi từ 250 mg cho tới 3 hoặc 4 g/ngày. Nó đặc biệt hiệu quả ở khối u ác tính mà không có chỉ định mổ. Tác dụng không mong muốn bao gồm phản xạ ngoại tháp và tinh thể niệu làm hạn chế việc sử dụng thuốc này. Khi phối hợp với phenoxybenzamin trong giai đoạn trước mổ, metyrosine có tác dụng tạo sự thuận lợi cho kiểm soát huyết động trong mổ.
Có thể sử dụng các thuốc ức chế kênh calci và thuốc ức chế men chuyển để kiểm soát tăng huyết áp. Calci là chất kích hoạt khối u tiết catecholamin và khi lượng lớn calci vào trong cơ tim góp phần gây ra bệnh lý cơ tim qua trung gian catecholamin. Phối hợp một thuốc ức chế beta 1 và một thuốc ức chế kênh calci (verapamil 120 mg – 240 mg mỗi ngày hoặc nifedipine 30 mg – 90 mg mỗi ngày) là một sự kết hợp có hiệu quả cho những trường hợp kháng thuốc.
– Giai đoạn trong mổ u tủy thượng thận
Các phẫu thuật có chuẩn bị được khuyến cáo bất cứ khi nào có thể. Chuẩn bị tối ưu trước mổ u tủy với thuốc ức chế anpha-adrenergic phối hợp hoặc không với thuốc ức chế beta-adrenergic và α-methylparatyrosin và cần điều trị hồi phục việc thiếu thể tích tuần hoàn. Mục tiêu của kiểm soát trong mổ bao gồm tránh sử dụng các thuốc hoặc các thao tác thô bạo có thể kích động tăng tiết catecholamin hoặc làm gia tăng tiềm lực hoạt động của catecholamin và duy trì sự ổn định về tim mạch với các thuốc tác dụng ngắn. Các thời điểm nguy hiểm nhất có thể gây tăng huyết áp thứ phát kèm theo rối loạn nhịp là lúc khởi mê, đặt ống nội khí quản, rạch da, mở bụng và đặc biệt trong khi lôi kéo khối u. Thời điểm buộc thắt tĩnh mạch của khối u cũng rất nguy hiểm vì gây hạ huyết áp thứ phát.
Theo dõi trong quá trình mổ gồm thiết bị theo dõi chuẩn cộng với theo dõi huyết áp động mạch xâm lấn, áp lực tĩnh mạch trung tâm, áp lực động mạch phổi qua catheter động mạch phổi và đặt sonde niệu đạo theo dõi nước tiểu. Nếu có thể theo dõi siêu âm tim qua thực quản để đánh giá chức năng cơ tim. Catheter động mạch cho phép theo dõi huyết áp động mạch dựa trên nhịp cơ bản, hơn nữa có thể lấy máu động mạch để làm các xét nghiệm cần thiết (như xét nghiệm hematocrit, hemoglobin, khí máu động mạch, đường máu). Một catheter tĩnh mạch trung tâm thường là đủ cho các bệnh nhân không có triệu chứng ở hệ tim mạch hoặc các dấu hiệu khác liên quan đến tim mạch. Catheter động mạch phổi có thể cần thiết để kiểm soát khi truyền một lượng dịch lớn, thiếu nhiều thể tích tuần hoàn và ở những bệnh nhân rối loạn chức năng cơ tim tiềm ẩn với các khối u hoạt động. Một lượng dịch lớn cần bù vào sau khi khối u được cắt bỏ cho thấy giảm mối quan hệ giữa thể tích và huyết áp do giảm đột ngột lượng catecholamin. Cần đảm bảo một lượng dịch trong cân bằng dương lớn để giữ thể tích nội mạch ở trong giới hạn bình thường.
Có thể sử dụng siêu âm trong mổ u tủy để xác định vị trí và chức năng các khối u tủy nhỏ và để thực hiện việc tách tuyến thượng thận hoặc cắt bán phần tuyến thượng thận. Quá trình tách tuyến thượng thận thực sự có giá trị khi cắt bỏ u tủy ở tuyến thượng thận hai bên. Phẫu thuật nội soi u tủy có thể được thực hiện khi kích thước khối u tủy nhỏ hơn 4 cm – 5 cm. Thường gặp tăng huyết áp khi bơm hơi ổ bụng cũng như khi kích thích trực tiếp vào khối u tủy.
Cả hai kỹ thuật vô cảm vùng và gây mê toàn thể đều đã được áp dụng thành công cho phẫu thuật cắt u tủy tuyến thượng thận. Các thuốc có thể gây đáp ứng tăng huyết áp thông qua:
+ Kích thích trực tiếp các tế bào khối u.
+ Kích thích hệ thần kinh giao cảm.
+ Tăng giải phóng các catecholamin dự trữ ở các tận cùng thần kinh.
+ Can thiệp vào sự thu nhận catecholamin của tế bào thần kinh.
+ Gây mẫn cảm các receptor catecholamin hoặc làm tăng hiệu quả tác dụng của catecholamin lên các tiểu động mạch.
Tất cả các thuốc gây mê đều đã được sử dụng với mức độ thành công khác nhau, về mặt lý thuyết một số thuốc cần tránh sử dụng để ngăn chặn đáp ứng bất lợi về mặt huyết động có thể xảy ra. Morphin và atracurium có thể gây tăng tiết histamin, có thể là yếu tố thúc đẩy tăng tiết catecholamin từ khối u. Các thuốc hủy phó giao cảm như atropin, pancuronium (Pavulon) và succinylcholin hoặc các thuốc kích thích thần kinh giao cảm đều có thể gây kích thích hệ thần kinh giao cảm. Mặc dù nồng độ cao halothan có hiệu quả cao trong việc làm suy giảm các đáp ứng biến đổi huyết động (như tăng huyết áp, tăng nhịp tim) với các kích thích vô cảm và phẫu thuật, nhưng nó lại làm tăng độ nhạy cảm của cơ tim với catecholamin nên cần tránh sử dụng. Droperidol, chlorpromazine, metoclopramide và ephedrin gây đáp ứng tăng huyết áp đáng kể. Các thuốc gây mê an toàn gồm thiopental, etomidate, các benzodiazepine, fentanyl, sufentanil, alfentanil, enfluran, isofluran, nitrous oxide, vecuronium và rocuronium. Mặc dù vậy, nhưng việc lựa chọn các thuốc gây mê không quan trọng bằng sự hiểu biết về thuốc nào sẽ được sử dụng. Các yếu tố kích thích tăng tiết catecholamin như là sự sợ hãi, căng thẳng, đau, run rẩy, thiếu oxy và tăng thán khí cần được giảm tới mức thấp nhất hoặc tránh ở giai đoạn trước, trong và sau mổ.
Gần như tất cả các bệnh nhân đều có biểu hiện tăng huyết áp động mạch tâm thu trên 200 mmHg giai đoạn trong mổ u tủy thượng thận cho dù đã dùng thuốc ức chế anpha từ trước mổ. Cần chuẩn bị một số thuốc hạ huyết áp và sẵn sàng sử dụng ngay khi cần thiết. Muối nitroprusside, một thuốc giãn mạch trực tiếp là thuốc được lựa chọn vì hiệu lực và khởi phát tác dụng ngay sau khi tiêm, thời gian tác dụng ngắn. Phentolamin, thuốc ức chế cạnh tranh anpha-adrenergic và gây giãn mạch trực tiếp rất hiệu quả mặc dù giảm nhanh tác dụng và gây nhịp chậm tim. Nitroglycerin cũng có hiệu quả nhưng nó đòi hỏi liều cao để kiểm soát những cơn tăng huyết áp và có thể gây nhịp nhanh tim. Labetalol có tác dụng ức chế beta nhiều hơn ức chế anpha được sử dụng nhiều hơn ở những bệnh nhân có khối u tăng tiết ưu thế epinephrin. Magnesium sulfat ức chế tiết catecholamin từ u tủy thượng thận và tận cùng thần kinh ngoại vi, làm giảm sự nhạy cảm của các receptor anpha với catecholamin và có tác dụng giãn mạch trực tiếp cũng như chống rối loạn nhịp tim. Tuy nhiên, cũng như các thuốc điều trị tăng huyết áp khác, nó không đạt được sự kiểm soát tăng huyết áp tối ưu khi kích thích khối u tủy thượng thận bằng tay. Sự phối hợp các thuốc điều trị tăng huyết áp như là nitroprusside, esmolol, diltiazem và phentolamine được sử dụng để kiểm soát tăng huyết áp khó điều trị. Tăng độ sâu gây mê cũng là một sự lựa chọn khi mổ u tủy mặc dù điều này có thể làm nặng thêm hạ huyết áp khi kẹp cắt tĩnh mạch khối u.
Rối loạn nhịp tim thường là xuất phát từ thất và được điều trị bằng lidocain hoặc các thuốc ức chế beta. Lidocain có tác dụng ngắn và ít ảnh hưởng tới sự co bóp cơ tim. Mặc dù propranolol được sử dụng rộng rãi nhưng esmolol (ức chế chọn lọc beta 1) mới là thuốc có nhiều ưu điểm hơn. Esmolol khởi phát tác dụng nhanh và thời gian tác dụng ngắn (thời gian bán thải là 9 phút), cho phép kiểm soát thích hợp nhịp tim và có tác dụng bảo vệ chống lại bệnh cơ tim và thiếu máu cơ tim do catecholamin cũng như chống lại sự hạ đường máu sau mổ. Amiodaron là thuốc chống loạn nhịp có tác dụng kéo dài điện thế hoạt động của cơ nhĩ và thất đã được sử dụng như thuốc thay thế ức chế beta (metoprolol) để điều trị nhịp nhanh trên thất do tăng cao catecholamin.
Thường có tụt huyết áp đáng kể sau khi kẹp thắt tĩnh mạch khối u tủy và thứ phát do sự kết hợp của các yếu tố bao gồm như giảm đột ngột nồng độ catecholamin huyết tương (nửa đời sống thải trừ của norepinephrine và epinephrine khoảng từ 1 – 2 phút), giãn mạch do tồn dư các thuốc ức chế anpha cùng với phenoxybenzamin, mất máu và dịch trong mổ và tăng độ sâu của gây mê. Huyết áp tâm thu tụt dưới 70 mmHg không thường xảy ra. Để dự phòng tụt huyết áp đột ngột, cần nâng áp lực giường mao mạch phổi lên 16 đến 18 mmHg trước khi kẹp cắt tĩnh mạch u tủy thượng thận. Thường sử dụng dung dịch ringer lactat hoặc nước muối sinh lý trước khi lấy bỏ khối u tủy và bổ sung dung dịch dextrose sau khi cắt u. Cần giảm độ sâu gây mê để góp phần kiểm soát huyết áp thấp. Sau khi cắt u tủy thượng thận gây ra hiện tượng giảm đột ngột nồng độ catecholamin huyết tương, kéo theo tăng mức insulin và giảm đường máu. Thường ít gây mất máu khi cắt u tủy tuyến thượng thận trong ổ bụng. Các thuốc co mạch (như phenylephrine, norepinephrine) và tăng sức bóp cơ tim (dopamine) cần sẵn sàng sử dụng nếu huyết áp thấp chậm đáp ứng với liệu pháp truyền dịch. Cần thiết bổ sung một lượng dịch thích hợp và đó là yếu tố chính làm giảm tỷ lệ tử vong trong mổ u tủy tuyến thượng thận. Các thuốc co mạch và tăng cường sức bóp cơ tim cần được xem như một phương thức điều trị thứ cấp. Sự tồn dư các thuốc ức chế anpha-adrenergic và giảm sự điều hòa các receptor khiến một số bệnh nhân ít đáp ứng với thuốc co mạch. Liệu pháp glucocorticoid cần được áp dụng nếu thực hiện cắt u tủy tuyến thượng thận hai bên hoặc có khả năng suy tuyến thượng thận.
– Giai đoạn sau mổ u tủy thượng thận
Phần lớn các bệnh nhân u tủy có huyết áp trở lại bình thường sau khi cắt bỏ hoàn toàn khối u. Mức catecholamin huyết tương chưa trở về bình thường cho tới tận ngày thứ 7 hoặc 10 sau mổ do có sự giải phóng dần dần catecholamin từ tận cùng các sợi thần kinh ngoại vi. Có khoảng 50% bệnh nhân tăng huyết áp một vài ngày sau mổ, có 25% – 30% bệnh nhân tăng huyết áp không hạn định. Tăng huyết áp này thường thấp hơn so với trước phẫu thuật và không có cơn tăng huyết áp kịch phát và không có các triệu chứng kinh điển của tăng catecholamin trong máu. Chẩn đoán phân biệt các bệnh nhân có tăng huyết áp dai dẳng với trường hợp chẩn đoán nhầm u tủy thượng thận, thiếu máu thận sau biến chứng của phẫu thuật và những bệnh nhân tăng huyết áp tiềm tàng.
Tụt huyết áp là nguyên nhân thường gặp nhất gây tử vong ngay trong giai đoạn sau phẫu thuật. Cần bổ sung lượng lớn dịch truyền vì các mạch máu ngoại vi không đáp ứng với giảm mức catecholamin. Hơn nữa, có sự mất dịch vào khoang thứ ba, tác dụng của phenoxybenzamine và α-methylparatyrosine tồn dư có thể kéo dài thời gian bán thải tới 36 giờ. Cần bổ sung steroid cho các bệnh nhân cắt u tuyến thượng thận hai bên hoặc nghi ngờ có suy tuyến thượng thận.
Có thể hạ đường máu vì tăng tiết quá mức insulin và phân giải mỡ, glycogen không thích hợp. Các thuốc ức chế không chọn lọc beta như propranolol có thể làm trầm trọng thêm việc hạ đường máu do giảm trương lực giao cảm và che giấu các triệu chứng của hạ đường máu. Truyền dung dịch chứa dextrose được coi là một phần trong truyền dịch liệu pháp và mức glucose máu cũng cần được theo dõi 24 giờ.
Các bệnh nhân u tủy thượng thận thường được lưu lại ICU ít nhất 24 giờ. Cần có chế độ kiểm soát đau thích hợp mặc dù có sự tăng nhạy cảm với các thuốc giảm đau morphin và ngủ gà. Nhu cầu kiểm soát thông khí dựa trên mức độ của phẫu thuật, vị trí phẫu thuật và tình trạng của bệnh nhân.
Tỷ lệ mắc bệnh có liên quan tới cắt bỏ u tuyến thượng thận khoảng 24% và tỷ lệ tử vong khoảng 2,4%. Sự hiểu biết sâu sắc về sinh lý bệnh khối u tủy thượng thận là điều quan trọng nhất để dự kiến kế hoạch vô cảm. Những tiến bộ mới đây về phương pháp chẩn đoán và định vị khối u tủy cũng như sự phát triển các thuốc mới điều trị hạ huyết áp trong tương lai sẽ góp phần chăm sóc và điều trị tốt hơn cho các bệnh nhân u tủy thượng thận.
Chuẩn bị bệnh nhân kỹ lưỡng trước mổ; có sự phối hợp tốt giữa bác sĩ nội khoa, bác sĩ nội tiết, phẫu thuật viên và bác sĩ gây mê; chuẩn bị đầy đủ và tỉ mỉ trong khi mổ; kiểm soát tốt tình trạng trước, trong và sau mổ là những điều cần thiết để thực hiện quá trình vô cảm phẫu thuật cho bệnh nhân u tủy thượng thận.
Yhocvn.net
BÀI CÙNG CHỦ ĐỀ:
+ Tăng huyết áp do u tủy thượng thận: triệu chứng phân biệt
Chưa có bình luận.